Arzneimittel
Tamoxifen Lieferengpass: Abgabe von Importen
Im März 2022 berichteten wir über den Lieferengpass bei tamoxifenhaltigen Arzneimitteln und die eingeleiteten Maßnahmen zur Versorgungssicherung.
Unter anderem wurde ein Import von 5 Millionen Tamoxifentabletten (20 mg) kurzfristig genehmigt und die verordnenden Praxen wurden gebeten, jeweils nur kleine Packungen (30 Stück) zu verordnen. Die empfohlene Verordnung und Abgabe von Kleinpackungen ist jedoch nun nicht mehr erforderlich, da sich die Versorgungslage mit tamoxifenhaltigen Arzneimitteln, laut Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM), wieder stabilisiert hat.
Um einen weiteren Engpass in der zweiten Jahreshälfte in der Versorgung zu vermeiden, hat das BfArM angeordnet, zunächst die importierten Tabletten durch die pharmazeutischen Großhändler in den Markt bringen zu lassen. Die Apotheken werden somit weiterhin importierte Ware abgeben. Bei der Verordnung großer Packungen (100 Stück) ist auch eine Bündelung aus kleinen importierten Packungen möglich. Die Anordnung des BfArM verliert ihre Wirksamkeit, wenn das BMG bekannt gibt, dass der Versorgungsmangel nicht mehr vorliegt.
Weitere Informationen dazu finden Sie auf der Infoseite des BfArM.
Zinkverbindungen – Klarstellung in Anlage I (OTC-Übersicht) der Arzneimittel-Richtlinie
In derAnlage I (OTC-Übersicht) der Arzneimittel-Richtlinie (AM-RL) sind die Ausnahmen aufgeführt, für die Verordnungen von apothekenpflichtigen Arzneimitteln zu Lasten der gesetzlichen Krankenversicherung vorgenommen werden dürfen.
In Nummer 45 der Anlage I wurde nun klargestellt, dass die ausnahmsweise Verordnungsfähigkeit von Zinkverbindungen als Monopräparate neben dem durch eine Haemodialysebehandlung bedingten Zinkmangel jetzt auch bei weiteren Dialyseverfahren, wie der Peritonealdialyse oder der Hämofiltration, gegeben ist. Im Sinne einer Vereinheitlichung hat der Gemeinsame Bundesausschuss (G-BA) die Regelung in Nummer 45 entsprechend angepasst: der Begriff „Haemodialysebehandlung“ wurde durch das Wort „Dialysebehandlung“ ersetzt. Die Gründe der G-BA Entscheidung finden Sie hier.
Der Beschluss ist am 4. Mai 2022 in Kraft getreten.
Bundesweite Praxisbesonderheit für Lynparza® erweitert
Für das Arzneimittel Lynparza® (Wirkstoff: Olaparib) wurde eine ab dem 1. März 2022 gültige Anerkennung der Verordnung des Arzneimittels als Praxisbesonderheit im Anwendungsgebiet „Monotherapie für die Behandlung von erwachsenen Patienten mit metastasiertem kastrationsresistentem Prostatakarzinom und BRCA1/2-Mutationen (in der Keimbahn und/oder somatisch), deren Erkrankung nach vorheriger Behandlung, die eine neue hormonelle Substanz (new hormonal agent) umfasste, progredient ist“ vereinbart.
Die seit 1. Juni 2019 gültige Anerkennung als Praxisbesonderheit im Anwendungsgebiet „Monotherapie für die Erhaltungstherapie von erwachsenen Patientinnen mit einem Platin-sensitiven Rezidiv eines high-grade epithelialen Ovarialkarzinoms, Eileiterkarzinoms oder primären Peritonealkarzinoms, die auf eine Platin-basierte Chemotherapie ansprechen (vollständig oder partiell)“ und seit 1. September 2020 gültige Anerkennung als Praxisbesonderheit im Anwendungsgebiet „Monotherapie für die Behandlung von erwachsenen Patienten mit BRCA1/2-Mutationen in der Keimbahn, die ein HER2-negatives, lokal fortgeschrittenes oder metastasiertes Mammakarzinom haben. Die Patienten sollten zuvor mit einem Anthrazyklin und einem Taxan im (neo)adjuvanten oder metastasierten Setting behandelt worden sein, es sei denn, die Patienten waren für diese Behandlungen nicht geeignet. Patienten mit Hormonrezeptor (HR)-positivem Mammakarzinom sollten außerdem eine Krankheitsprogression während oder nach einer vorherigen endokrinen Therapie aufweisen oder für eine endokrine Therapie nicht geeignet sein“ bleibt weiter bestehen.
Auf der Website der KV Berlin unter „Wirtschaftlichkeitsprüfung“ sind die bestehenden bundesweiten Praxisbesonderheiten aufgeführt. Bei Einhaltung der zwischen GKV-Spitzenverband und dem jeweiligen pharmazeutischen Unternehmen vereinbarten Bedingungen werden diese Arzneimittel im Rahmen einer Durchschnittswerteprüfung von den Verordnungskosten abgezogen.
Heilmittel
Neues Heilmittel: Nagelspangenbehandlung
Der Gemeinsame Bundesausschuss (G-BA) hat bereits im Februar eine Änderung der Heilmittel-Richtlinie dahingehend beschlossen, dass ab dem 1. Juli 2022 die Nagelspangenbehandlung bei eingewachsenen Zehennägeln (Unguis incarnatus, ICD-10-Code L60.0) in den Stadien 1 bis 3 als Heilmittel verordnungsfähig ist. Der Beschluss des G-BA ist zwischenzeitlich bereits im Bundesanzeiger veröffentlicht (BAnz AT 07.04.2022 B2). Die Heilmittel-Stammdaten für die Softwareanbieter werden im Mai 2022 aktualisiert.
Hintergrund
Die Behandlung eingewachsener Zehennägel mit Hilfe einer Nagelkorrekturspange ist ein konservatives Verfahren, welches bisher ausschließlich in den Sicherstellungsbereich der Vertragsärzt:innen fiel, wobei die Vergütung bereits in der Versicherten- und Grundpauschale enthalten war, da die Nagespangenbehandlung im EBM in Anlage 1 (als nicht gesondert berechnungsfähige Leistungen) aufgeführt war. Das Bundessozialgericht (BSG) urteilte bereits Ende 2018, dass die Nagelspangenbehandlung eine ärztliche Leistung sei, die nicht durch Podologen erbracht werden könne (AZ: B 1 KR 34/17 R). Da keine Ärzt:innen diese Leistung erbringen würden und die Nagelspangenbehandlung auch nicht verordnet werden könne, so das BSG, läge ein Systemversagen vor. Bisher wurde die Nagelspangenbehandlung allenfalls durch Podolog:innen erbracht, und über ein Kostenerstattungsverfahren mit den Krankenkassen der Patient:innen abgerechnet.
In der Folge leitete der G-BA im Mai 2020 ein Beratungsverfahren dazu ein. Ziel war, die Nagelspangenkorrektur als Heilmittel verordnungsfähig zu machen und so eine Leistungserbringung durch Podolog:innen zu ermöglichen.
Nagelspangenbehandlung in der Heilmittel-Richtlinie und im Heilmittelkatalog
Die Heilmittel-Richtlinie wurde um einen neuen Abschnitt „podologische Therapie bei Unguis incarnatus: Behandlung mit Nagelkorrekturspangen (Orthonyxiespangen)“ ergänzt. Im Zuge dessen erfolgte eine Umstrukturierung, sodass nun drei neue Paragraphen die folgenden Inhalte regeln:
- § 28 – Behandlungsziel und Verordnungsvoraussetzungen
- § 28a – Zusammenarbeit und Qualitätssicherung
- § 28b – Inhalt der Nagelspangenbehandlung
Im Heilmittelkatalog wurden im neuen Abschnitt „Nagelkorrekturspangen bei Unguis Incarnatus“ die folgenden beiden Diagnosegruppen ergänzt:
- UI1 – Unguis incarnatus Stadium 1
- UI2 – Unguis incarnatus Stadium 2 und 3
In Diagnosegruppe UI1 sind bis zu acht Einheiten je Verordnung möglich, in Diagnosegruppe UI2 sind es vier Einheiten. Die Unterscheidung ist notwendig, um in schwereren Erkrankungsstadien eine häufigere ärztliche Wiedervorstellung zu gewährleisten.
Sicherung der Behandlungsqualität
Es wurde durch den G-BA klargestellt, dass sich die Behandlung durch Podolog:innen auf die Anlage, Nachregulierung und Entfernung der Nagelkorrekturspange beschränkt – Diagnostik und konservative oder invasive Maßnahmen der Wundbehandlung sind weiterhin Ärzt:innen vorbehalten. Eine Befestigung der Nagelkorrekturspange muss ohne weitergehende Verletzung der geschädigten Haut oder des Weichteilgewebes möglich sein. Insbesondere bei Stadium 2 und 3 muss die Behandlung in enger Abstimmung mit den Ärzt:innen erfolgen und es muss vor Beginn der Behandlung, bei einer Verschlechterung des Krankheitsbildes sowie nach Abschluss der Behandlung eine Fotodokumentation erfolgen.
Bitte beachten Sie: Zwar wurden mit der Aufnahme der Nagelspangenbehandlung in die Heilmittel-Richtlinie die notwendigen Grundlagen für eine Verordnung geschaffen, jedoch stehen die Anpassungen der Rahmenverträge nach § 125 SGB V zwischen den Spitzenverbänden der Podologen und dem GKV-Spitzenverband noch aus. Es ist den Podolog:innen daher derzeit noch nicht möglich, eine Nagelspangenkorrektur zu erbringen.
Heilmittel: Telemedizinische Leistungen
Eine kürzlich in Kraft getretene Ergänzungsvereinbarung zwischen dem GKV-Spitzenverband und den Spitzenverbänden der Physiotherapeuten ermöglicht (rückwirkend zum 1. April 2022) weiterhin die Erbringung physiotherapeutischer Leistungen als Videobehandlung unabhängig von den pandemiebedingten Sonderregelungen. Hintergrund ist das Gesetz zur digitalen Modernisierung von Versorgung und Pflege (DVPMG), welches einen Anspruch von Versicherten auf telemedizinische Erbringung von Heilmitteln begründet (§ 32 Abs. 1 Satz 2 SGB V).
Nachdem übergangsweise eine Videobehandlung in den Bereichen Physio-, Ergo- sowie Stimm-, Sprech-, Sprach- und Schlucktherapie und der Ernährungstherapie aufgrund der pandemischen Lage möglich war, wurde nun zunächst die Videobehandlung im Bereich Physiotherapie in die Regelversorgung überführt. In den weiteren Heilmittelbereichen konnte diesbezüglich bisher noch keine Einigung erzielt werden. Im Bereich Ernährungstherapie ist künftig die Anamnese und die Intervention per Video möglich, jedoch dürfen nicht mehr als die Hälfte des verordneten Zeitkontingents per Video erbracht werden. Bis zu 30 Minuten sind als telefonische Beratung möglich.
Videobehandlung im Bereich Physiotherapie
Ob eine verordnete Physiotherapie auch als telemedizinische Leistung erbracht werden darf, entscheiden Sie als verordnende Ärzt:innen selbst. Ist eine telemedizinische Erbringung aus ärztlicher Sicht möglich, bedarf es zunächst keiner weiteren Angaben – sollten Sie dies jedoch ausschließen wollen, ist ein Hinweis im Feld „ggf. Therapieziele/weitere med. Befunde und Hinweise“ notwendig. Wird im Verlauf der Therapie ersichtlich, dass eine Videobehandlung möglich und geeignet ist, kann diese nach Zustimmung der Patient:innen und in Ihrem Einvernehmen (Änderung der Verordnung durch die Physiotherapeut:innen ohne erneute Unterschrift) auch telemedizinisch erbracht werden.
Die Entscheidung zur Physiotherapie als Videobehandlung wird zwischen den Patient:innen und den Therapeut:innen getroffen und muss in Echtzeit erfolgen. Die erste Behandlung sowie Verlaufskontrollen müssen jedoch im unmittelbaren persönlichen Kontakt erfolgen. Dies gilt auch, wenn das Therapieziel durch die Videobehandlung nicht erreicht werden kann, oder technische Probleme bestehen (siehe § 16b HM-RL). Das Angebot telemedizinischer Leistungen ist für die Physiotherapiepraxen freiwillig und darf ausschließlich in den zugelassenen Praxisräumen erfolgen. Das Einverständnis der Patient:innen zur Videobehandlung muss nach entsprechender Aufklärung schriftlich mit den Therapeut:innen vereinbart werden. Darüber hinaus soll die Behandlung immer von denselben Therapeut:innen durchgeführt werden – sowohl im direkten persönlichen, wie auch im telemedizinischen Kontakt (siehe § 7 der Ergänzungsvereinbarung).
Physiotherapeutische Leistungen als Videotherapie
Es dürfen nur bestimmte Heilmittel als telemedizinische Leistungen erbracht werden. Darüber hinaus ist der Anteil der Videotherapie an der Gesamtanzahl der Behandlungseinheiten eingeschränkt:
| Heilmittel | Behandlungseinheiten als Videotherapie |
| Allgemeine Krankengymnastik (KG) in Einzelbehandlung |
Höchstens die Hälfte der verordneten Behandlungseinheiten können als Videotherapie erbracht werden. |
| Allgemeine Krankengymnastik (KG) in Gruppenbehandlung | |
| Krankengymnastik zur Behandlung schwerer Erkrankungen der Atmungsorgane (KG Muko) | |
| KG-ZNS-Kinder nach Bobath | Höchstens drei der verordnetenn Behandlungseinheiten können als Videotherapie erbracht werden (insbesondere für die Anleitung der Bezugspersonen). |
| KG-ZNS-Erwachsene nach Bobath | |
| Manuelle Therapie | Höchstens eine Einheit der verordneten Behandlungseinheiten können als Videotherapie erbracht werden. |
Für die Physiotherapeut:innen wurden im bundeseinheitliche Positionsnummernverzeichnis neue Positionsnummern für die Abrechnung der telemedizinischen Leistungen eingeführt. Es gelten dabei die gleichen Preise, die auch bei einer Behandlung in der Praxis abgerechnet werden würden.
Sprechstundenbedarf
Elektronische Bestellung des Sprechstundenbedarfs – erneute Informationen zur Bearbeitung durch die AOK Nordost im Portal der KV Berlin
Die Anforderung von Sprechstundenbedarf erfolgt seit Jahresanfang ausschließlich elektronisch über das Online-Portal der KV Berlin. Eine Schritt-für-Schritt-Anleitung zur Anmeldung im Online-Portal und zur Bestellung finden Sie im KV-Blatt 01/2022 (ab Seite 52).
Aufgrund vermehrter Anfragen zur Rückmeldung der AOK Nordost haben wir Ihnen einige Hinweise zusammengestellt.
Für den apothekenpflichtigen Sprechstundenbedarf:
- sobald die Bearbeitung der Bestellung zum apothekenpflichtigen Sprechstundenbedarf durch die AOK Nordost erfolgt ist, erhalten Sie eine E-Mail über das Portal der KV Berlin (*1)
- nach dem Login über das KV Berlin Portal wird die Bestellung dann als grüne Bestellzeile angezeigt (*2)
- durch Anklicken des i (siehe Pfeil) gelangen Sie in die Detailansicht (*3)
- beim apothekenpflichtigen SSB muss das Schreiben (siehe Pfeil) als PDF heruntergeladen, ausgedruckt, vom Arzt oder der Ärztin unterschrieben und abgestempelt werden
- danach geben Sie das PDF bitte an die angegebene Apotheke, um die Artikel zu erhalten
Für den nichtapothekenpflichtigen Sprechstundenbedarf:
- sobald die Bearbeitung der Bestellung zum nichtapothekenpflichtigen Sprechstundenbedarf durch die AOK Nordost erfolgt ist, erhalten Sie eine E-Mail (*1)
- die Bestellung wird dann im Online-Portal als grüne Bestellzeile angezeigt (*2)
- durch Anklicken des i (siehe Pfeil) gelangen Sie in die Detailansicht
- der nichtapothekenpflichtige SSB wird Ihnen automatisch zugesendet
- die Detailansicht des NAPO-SSB zeigt Ihnen die beauftragten Lieferanten (*4)
- eine Bestätigung der Lieferung der NAPO-Artikel, per Fax an die AOK Nordost, ist seit letztem Jahr nicht mehr nötig
*1 - Information per E-Mail
*2 - Anzeige im Online-Portal (Übersichtsseite)
*3 - Anzeige im Online-Portal (Detailansicht APO-SSB)

Wurden Kürzungen oder Streichungen vorgenommen mit denen Sie nicht einverstanden sind? Dann wenden Sie sich an die AOK Nordost oder die Verordnungsberatung der KV Berlin.
*4 - Anzeige im Online-Portal (Detailansicht NAPO-SSB)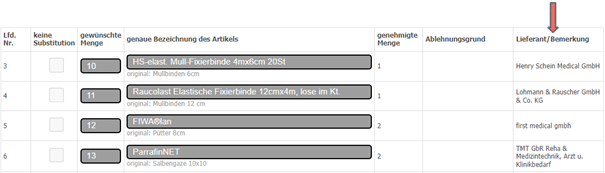
Bei fehlenden oder falsch gelieferten NAPO-Artikeln wenden Sie sich bitte an die AOK-Nordost. Bei unklaren Ablehnungsgründen, Mengenkürzungen oder der Suche nach Alternativen, wie bei „Außer Handel“- Artikeln kontaktieren Sie uns unter verordnung@kvberlin.de.
Bitte beachten Sie zudem, dass die momentanen Bearbeitungszeiten beim apothekenpflichtigen Sprechstundenbedarf ca. fünf bis sechs Wochen betragen können. Falls Sie zeitlich dadurch in Versorgungsschwierigkeiten geraten würden, melden Sie dies bitte bei der AOK Nordost und bitten um bevorzugte Bearbeitung.
Wirtschaftlichkeitsprüfung
Erneute Schreiben von Krankenkassen zu Aut-idem-Kreuzen auf Muster 16
Abermals gehen Schreiben von Krankenkassen, mit einem vermeintlichen Informations- und Unterstützungscharakter bei Berliner Arztpraxen ein. Zudem wird in den Schreiben ein entsprechender Anruf der Krankenkasse bei der Praxis avisiert.
Verbunden mit dem Hinweis zur wirtschaftlichen Verordnungsweise, weisen die Krankenkassen auf eine Überschreitung einer kassenintern ermittelten Aut-idem-Quote ihrer Fachgruppe hin.
Hinweise Ihrer KV zu diesem Vorgehen:
Den Gesetzlichen Krankenkassen ist seit 1. April 2020, durch die Änderung des § 305a Sozialgesetzbuch Fünf (SGB V) untersagt, Ärzt:innen zur wirtschaftlichen Verordnungsweise zu beraten. Kassenindividuell ermittelte Quoten können keine belastbare Aussage darüber treffen, ob die Gesamtverordnungen wirtschaftlich sind oder nicht.
In den Schreiben der verschiedenen Kassen wird die Regelung nach § 40 Abs. 3 der Arzneimittel-Richtlinie zitiert.
Wichtig zu wissen:
Die Regelung der Arzneimittel-Richtlinie skizziert keine Verpflichtung zum Verzicht auf das Aut-idem-Kreuz, sondern lautet: „Die Möglichkeit der verordnenden Ärztin oder des verordnenden Arztes, unter Würdigung patientenindividueller und erkrankungsspezifischer Aspekte nach § 73 Absatz 5 Satz 2 SGB V die Ersetzung durch ein wirkstoffgleiches Arzneimittel auszuschließen, bleibt von diesen Regelungen unberührt.“
Um den Austausch gegen wirkstoffgleiche Mittel auszuschließen, bedarf es medizinischer patientenindividueller Gründe. Diese sollten in der Patientenakte dokumentiert werden. Im Falle einer Einzelfallprüfung, die durch die Krankenkassen per Antrag bei der Prüfungsstelle initiiert werden können, wäre dies relevant.
In den, der Wirtschaftlichkeitsprüfung zugrundeliegenden, Regularien gibt es keine definierten Quoten oder Ziele zum Aut idem. Das Zulassen des Austausches von verordneten Arzneimitteln gegen „ein Gleiches“ stellt jedoch ein probates Mittel im Rahmen des Wirtschaftlichkeitsgebotes dar.
Die Angebote zur telefonischen Beratung müssen Sie keinesfalls wahrnehmen.
Ergänzende Informationen:
In Anlage VII der Arzneimittel-Richtlinie, hat der Gemeinsame Bundesausschuss
- unter Teil A die Wirkstoffe der aktuell austauschbaren Darreichungsformen und
- unter Teil B Wirkstoffe in der jeweiligen Darreichungsform festgelegt, für die ein generelles Austauschverbot gilt.
In Teil B werden vor allem Arzneimittel mit geringer therapeutischer Breite (§ 129 Abs. 1a Satz 2 Sozialgesetzbuch Fünf) berücksichtigt, bei denen schon eine geringfügige Änderung der Dosis oder Konzentration des Wirkstoffs zu klinisch relevanten Abweichungen in der angestrebten Wirkung oder zu schwerwiegenden unerwünschten Wirkungen führt.
Hinweis zur Verordnung:
Eindeutige Verordnung: Arzneimittel der Substitutionsausschlussliste müssen eindeutig verordnet werden, da jeglicher Austausch dieser Arzneimittel verboten ist. Der Name des Präparates, ggf. inklusive Hersteller, und die Pharmazentralnummer (PZN) definieren das gewünschte Arzneimittel genau.
- Kein Aut-idem-Kreuz erforderlich: Das Setzen des Aut-idem-Kreuzes ist beim Verordnen von Arzneimitteln der Substitutionsausschlussliste überflüssig, da sie von der Austauschpflicht gegen Rabattarzneimittel ausgenommen sind.
- Dokumentation: Damit der Patient identische Folgeverordnungen erhält, sollten die verordneten Präparate der Aut-idem-Liste in der Patientenakte sorgfältig dokumentiert werden.
Sonstiges
Doppelverordnung von Hilfsmitteln / Wechselversorgung
Hilfsmittelverordnungen zulasten der Gesetzlichen Krankenversicherung unterliegen, wie auch die Arzneimittelverordnungen, dem Wirtschaftlichkeitsgebot. Dies bedeutet, dass die Verordnungen notwendig, zweckmäßig und ausreichend sein müssen. Ableitend daraus ist eine Mehrfachausstattung mit dem gleichen Hilfsmittel nicht grundsätzlich zulässig.
Ärzt:innen können, gemäß § 6 Absatz 8 der Hilfsmittel-Richtlinie, funktionsgleiche Mittel mehrfach verordnen, wenn dies aus medizinischen, hygienischen oder sicherheitstechnischen Gründen notwendig oder aufgrund der besonderen Beanspruchung durch die Patient:innen zweckmäßig und wirtschaftlich ist. Hinweise zu einer sogenannten Doppel- oder Wechselversorgung ergeben sich unter anderem aus den Definitionen oder in der Beschreibung zur jeweiligen Produktgruppe bzw. Produktart im Hilfsmittelverzeichnis. Bitte prüfen Sie die Mehrfachausstattung je Einzelfall.
Ein gängiges Beispiel ist die Versorgung mit Kompressionsstrümpfen (Produktgruppe – PG-17) oder Prothesen-BHs (PG 37). Bei diesen Produkten ist in der Regel allein aus hygienischen Gründen eine sogenannte zeitgleiche Verordnung der Wechselversorgung angebracht. Bei Kompressionsstrümpfen kann zunächst auch ein Paar verordnet werden, um sich von der Zweckmäßigkeit, Passgenauigkeit und Handhabbarkeit durch die Patient:innen zu überzeugen. Die Zuschüsse zu den Epithesen-BHs sind je Krankenkasse unterschiedlich. Informationen dazu erhalten die Patientinnen bei ihrer Krankenkasse.
Auch bei orthopädischen Straßenschuhen (PG 31) kann eine zeitgleiche Verordnung zur Wechselversorgung angebracht sein. Informationen dazu finden Sie unter den Definitionen in den Abschnitten zu den einzelnen Produktarten. So können Patient:innen, um ihren Bedürfnissen ausreichend Rechnung zu tragen und aus hygienischen Gründen, nach der erstmaligen Versorgung mit einem Paar grundsätzlich ein weiteres Wechselpaar erhalten, wenn das erste Paar mindestens vier Wochen als passgerecht und funktionsfähig erprobt wurde. Bei orthopädischen Haus-, Sport- und Badeschuhen ist in der Regel keine Versorgung mit einem Wechselpaar aus hygienischen Gründen erforderlich.
Weiterhin gibt es entsprechende Hinweise z. B. auch für die Verordnung von Blindenlangstöcken. In der Beschreibung unter der jeweiligen Produktart (z.B. 07.50.01.0-Einteilige Langstöcke) wird klargestellt: „Eine erstmalige Verordnung eines Blindenlangstocks erfolgt i. d. R. mit einer Schulung in Orientierung und Mobilität. Die Erstausstattung umfasst meist zwei Langstöcke.“
Hilfsmittelverordnungen sind für die statistische Vergleichsprüfung (Durchschnittswerteprüfung) nicht relevant, können jedoch im Rahmen von Einzelprüfanträgen der Krankenkassen einer Wirtschaftlichkeitsprüfung durch die Prüfungsstelle unterzogen werden.


