Arzneimittel
Wichtige Aktualisierungen zur RSV-Prophylaxe mit Beyfortus® für Kinder
Nachfolgend finden Sie Informationen zu den Anspruchsberechtigten, RSV-Saison-Definition und Zeitpunkt der Gabe, ergänzend zu den letzten Praxis-News vom 18.09.2024 zu diesem Thema:
Anspruchsberechtigte
- Neugeborene und Säuglinge im ersten Lebensjahr
- vor ihrer ersten RSV-Saison
oder - innerhalb ihrer ersten RSV-Saison (siehe „Definition erste RSV-Saison“)
- vor ihrer ersten RSV-Saison
- Kinder im Alter von bis zu 24 Monaten
- die während ihrer zweiten RSV-Saison weiterhin anfällig für eine schwere RSV-Erkrankung sind:
- bronchopulmonale Dysplasie die begleitende therapeutische Maßnahmen (z. B. Sauerstoff, Steroide, Bronchodilatatoren, Diuretika) innerhalb der letzten sechs Monate vor Beginn der RSV-Saison benötigten
oder - mit hämodynamisch relevanten Herzfehlern (z. B. Links-Rechts- oder Rechts-Links-Shunt, pulmonale Hypertonie, pulmonalvenöse Stauung)
oder - mit Trisomie 21
- bronchopulmonale Dysplasie die begleitende therapeutische Maßnahmen (z. B. Sauerstoff, Steroide, Bronchodilatatoren, Diuretika) innerhalb der letzten sechs Monate vor Beginn der RSV-Saison benötigten
- die während ihrer zweiten RSV-Saison weiterhin anfällig für eine schwere RSV-Erkrankung sind:
Definition erste RSV-Saison
Das Pharmaunternehmen Sanofi hat der Kassenärztlichen Bundesvereinigung (KBV) bestätigt, dass auch für Kinder, die sich rein kalendarisch in der zweiten RSV-Saison befinden, nach Expositionsgesichtspunkten aber erst in ihrer ersten RSV-Saison sein könnten, ein zulassungskonformer Einsatz vorliegt. Damit ist eine RSV-Prophylaxe mit Nirsevimab zulasten der gesetzlichen Krankenversicherung (GKV) auch für diese älteren Babys im ersten Lebensjahr möglich (also Geburt vor dem 01.04.2024). Damit ist auch die Rechtsverordnung des Bundesgesundheitsministeriums inhaltlich zutreffend.
Nichtanspruchsberechtigte
- Säuglinge die sich bereits in ihrer zweiten RSV-Saison befinden (siehe „Definition erste RSV-Saison“)
- Kinder bis zu 24 Monaten ohne die Anfälligkeit für schwere RSV-Erkrankungen
Wann soll die Prophylaxe erfolgen?
- Neugeborene (April bis September) möglichst vor Beginn ihrer ersten RSV-Saison (idealerweise von September bis November)
- Neugeborene (Oktober bis März) möglichst zeitnah nach der Geburt
Verordnung und Bezug von Nirsevimab
- Verordnung als eRezept auf Namen der Patient:innen zulasten der jeweiligen Krankenkasse
- Zurzeit nicht über Sprechstundenbedarf -> sobald der Bezug über den SSB möglich ist informieren wir Sie!
- Sofern noch keine Versicherungsnummer für das Kind vorliegt, ohne Versichertennummer mit den Daten des Kindes verordnen (Papierrezept)
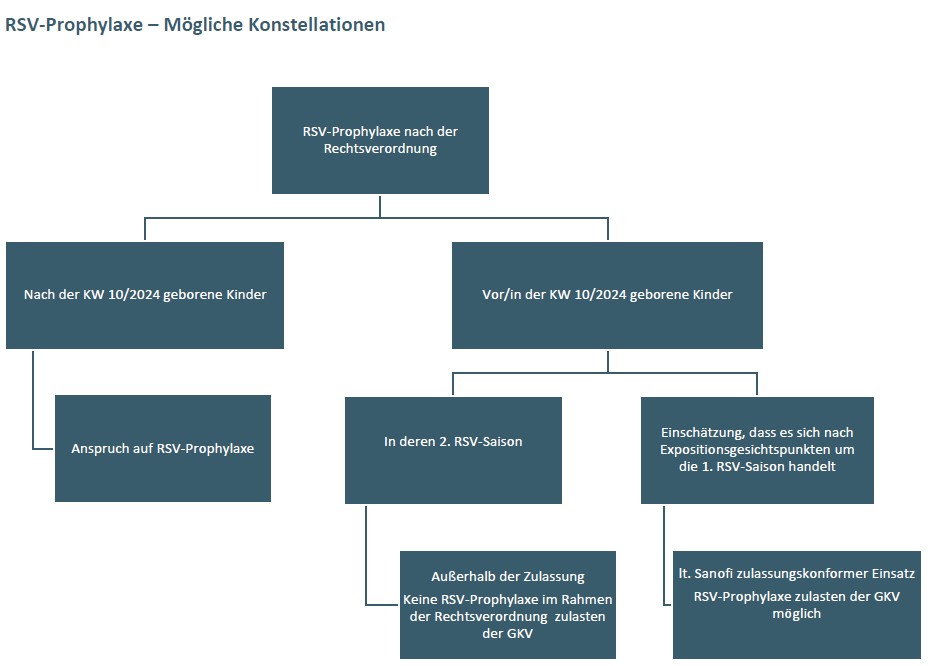
Quelle: KBV
Abrechnung
Der Erweiterte Bewertungsausschuss (EBA) hat für die Vergütung für die Prophylaxe gegen RSV folgende Gebührenordnungspositionen (GOP) seit dem 16. September 2024 beschlossen:
- 01941 Prophylaxe gegen RSV gemäß § 1 RSV-Prophylaxeverordnung – einmal im Krankheitsfall (75 Punkte / 8,95 Euro)
- nur bei Versicherten bis zum vollendeten ersten Lebensjahr, sofern noch keine RSV-Prophylaxe mit Nirsevimab in der RSV-Saison durchgeführt wurde
- Aufklärung und Beratung der Eltern beziehungsweise der Personensorgeberechtigten des Neugeborenen oder Säuglings zu Sinn, Zweck und Ziel der RSV-Prophylaxe. Hierzu gehören auch Informationen zum Wirkmechanismus eines monoklonalen Antikörpers – im Vergleich zu Impfstoffen, die im Rahmen der SI-RL des G-BA appliziert werden
- weitere Voraussetzung: intramuskuläre Injektion des Wirkstoffs Nirsevimab -> die Berechnung der GOP 01941 ohne Durchführung der RSV-Prophylaxe mit Nirsevimab ist nicht möglich
- die Dokumentation der erfolgten RSV-Prophylaxe in den Unterlagen des Neugeborenen bezie-hungsweise Säuglings, zum Beispiel im Impfausweis auf der Seite „Passive Immunisierung“, ist Bestandteil der GOP 01941
- 01942 Zuschlag zu der Gebührenordnungsposition 01941 für zusätzliche Aufgaben im Rahmen der Injektion der RSV-Prophylaxe gemäß § 1 RSV-Prophylaxeverordnung – einmal im Krankheitsfall (34 Punkte / 4,06 Euro)
- Die Gebührenordnungsposition 01942 wird durch die KV Berlin automatisch zugesetzt.
- nicht berechnungsfähig, sofern der monoklonale Antikörper Nirsevimab gegebenenfalls als Sprechstundenbedarf auf Basis der regional zu vereinbarenden Sprechstundenbedarfsvereinbarung bezogen werden kann
- 01943 Beratung und Aufklärung zur Prophylaxe gegen RSV gemäß § 1 RSV-Prophylaxeverordnung ohne nachfolgende intramuskuläre Injektion – einmal im Krankheitsfall (32 Punkte / 3,82 Euro).
- nur bei Versicherten bis zum vollendeten ersten Lebensjahr, sofern noch keine RSV-Prophylaxe mit Nirsevimab in der RSV-Saison durchgeführt wurde
- kann im Laufe von vier Quartalen (unter Einschluss des aktuellen Quartals) nur von einem Vertragsarzt einmalig abgerechnet werden
Diese GOP können ausschließlich durch folgende Vertragsärzt:innen abgerechnet werden:
- Hausärzt:innen
- Fachärzt:innen für Kinder- und Jugendmedizin
Wegfall der Vorabgenehmigung für Cannabis bei bestimmten Facharztgruppen
Der Beschluss des Gemeinsamen Bundesausschusses (G-BA) zum Wegfall der Vorabgenehmigungspflicht trat am 17.10.2024 in Kraft.
Wir hatten Sie dazu ausführlich in den Verordnungs-News Juli 2024 informiert.
Hier nochmal die Schwerpunkte:
- Ärzt:innen bestimmter Facharzt-, Schwerpunkt- oder Zusatzbezeichnungen dürfen seit dem 17.10.2024 medizinisches Cannabis ohne Genehmigung der gesetzlichen Krankenkassen verordnen
- bei Unsicherheiten, ob bei Patient:innen die Voraussetzungen für eine Cannabisverordnung erfüllen, kann weiterhin eine Genehmigung der Cannabisverordnung bei der Krankenkasse beantragt werden
- Ärzt:innen auf die keine der gelisteten Facharzt-, Schwerpunkt- oder Zusatzbezeichnung zutreffen, können weiterhin Cannabisprodukte nur unter vorheriger Genehmigung der Krankenkasse verordnen
Weiterhin gelten die grundsätzlichen Voraussetzungen von medizinischem Cannabis als Leistung der gesetzlichen Krankenversicherung
- nur möglich bei Versicherten mit einer schwerwiegenden Erkrankung,
- wenn eine andere allgemein anerkannte, dem medizinischen Standard entsprechende Behand-lungsoption nicht zur Verfügung steht
- und wenn Aussicht auf einen positiven Effekt von Cannabisarzneimitteln auf den Krankheitsverlauf oder schwerwiegende Symptome besteht.
Nähere Informationen des G-BA zur Verordnung von medizinischem Cannabis finden Sie hier: Antworten auf häufig gestellte Fragen.
Arzneimittel zur Eisensubstitution als GKV-Leistung
Für eine Verordnung von apothekenpflichtigen, nicht verschreibungspflichtigen Arzneimitteln mit Eisen-(II)-Verbindungen zu Lasten der gesetzlichen Krankenversicherung beschreibt die Anlage I der Arzneimittel-Richtlinie (AM-RL) die zu erfüllenden Voraussetzungen für Patient:innen ab 12 Jahren (und Patient:innen mit Entwicklungsstörungen ab 18 Jahren).
Eine Kassenleistung ist für die genannte Altersgruppe demnach für Monopräparate wie z. B. Tardyferon® oder Ferro Sanol® bei gesicherter Eisenmangelanämie gegeben, nicht jedoch für Kombinationspräparate wie z. B. Tardyferon®-Fol, Ferro Sanol® Comp und Ferro Sanol® Gyn.
Neben Möglichkeiten, den Eisenmangel durch orale Arzneiformen zu kompensieren, stehen auch ver-schreibungspflichtige Monopräparate mit Eisen-(III)-Verbindungen zur Injektion oder Infusion zur Verfügung (z. B. Ferrlecit®, Ferinject®, Monofer®). Diese sind überwiegend zugelassen, wenn eine orale Eisensubstitution nicht möglich oder unwirksam ist und unter Berücksichtigung der Angaben in der jeweiligen Fachinformation (Achtung: unterschiedliche Alterszulassungen!) Leistung der Gesetzlichen Krankenversi-cherung.
Bitte beachten Sie: Vor der Verordnung der Eisen-(III)-Verbindungen zur Injektion oder Infusion zu Kas-senlasten, haben aufgrund des Wirtschaftlichkeitsgebots rezeptfreie orale Eisen-(III)-Verbindungen Vorrang. Da die Anlage I der AM-RL die Eisen-(III)-Verbindungen nicht umfasst, besteht für diese Präparate kein Leistungsanspruch zu Kassenlasten. Erst wenn orale Eisen-(II)- und Eisen-(III)-Präparate ausgeschlossen bzw. nicht vertragen wurden oder zum Therapieziel führten, können verschreibungspflichtige parenterale Eisen-(III)-Verbindungen zu Lasten der Krankenkasse verordnet werden.
Zudem sind für alle Altersgruppen die verschreibungspflichtigen Antianämika-Kombinationen durch die Anlage III der Arzneimittel-Richtlinie von einer Verordnung zu Kassenlasten ausgeschlossen (siehe oben genannte Kombinationspräparate). Nicht verschreibungspflichtige Antianämika-Kombinationen sind ebenfalls für alle Altersgruppen keine Kassenleistung.
Eine Zuzahlungsbefreiung besteht gemäß Mutterschafts-Richtlinien bei Schwangerschaftsbeschwerden und im Zusammenhang mit der Entbindung.
Die Empfehlungen der Kassenärztlichen Bundesvereinigung und das Ablaufschema zur Labordiagnostik bei Eisenmangel und Anämie finden Sie hier.
Bundesweite Praxisbesonderheiten – Update
Neu: Libtayo® und Pombiliti®
Für diese Arzneimittel wurden bundesweite Praxisbesonderheiten vereinbart:
- Libtayo® (Wirkstoff Cemiplimab) seit 1. Mai 2024
- Pombiliti® (Wirkstoff Cipaglucosidase alfa) seit 1. Februar 2024
Für diese Arzneimittel werden die Verordnungskosten im Rahmen einer Durchschnittswerteprüfung von den Verordnungskosten der Praxis abgezogen. Voraussetzung ist dabei, dass die zwischen GKV-Spitzenverband und dem jeweiligen pharmazeutischen Unternehmen vereinbarten Bedingungen für eine bundesweite Praxisbesonderheit eingehalten werden.
Ablauf: Revestive® und Dacogen®
Die nachfolgenden bundesweiten Praxisbesonderheiten sind ausgelaufen:
- Revestive® (Wirkstoff: Teduglutid) Ablauf des Patentschutzes zum 05. September 2022 (Aktuali-sierung Internetseite des GKV-Spitzenverbandes am 05.09.2024)
- Dacogen® (Wirkstoff: Decitabin) Ablauf des Patentschutzes zum 25. September 2024 (Aktualisie-rung Internetseite des GKV-Spitzenverbandes am 25.09.2024)
Auf der Internetseite der KV Berlin sind alle gültigen und ausgelaufenen bundesweiten Praxisbesonderheiten, die der GKV-Spitzenverband bereits stellt, aufgeführt.
Verlängerung der Verordnungsfähigkeit von Medizinprodukten (Anlage V AM-RL)
Die nach der Arzneimittel-Richtlinie (AM-RL) zu Lasten der gesetzlichen Krankenversicherung (GKV) verordnungsfähigen Medizinprodukte, inklusive der medizinisch notwendigen Fälle, sowie der jeweiligen zeitlichen Befristung für die Erstattung, sind in der Anlage V der AM-RL aufgeführt.
Die Bestimmungen der Anlage V AM-RL gelten auch für versicherte Kinder bis zum vollendeten 12. Lebensjahr und versicherte Jugendliche mit Entwicklungsstörungen bis zum vollendeten 18. Lebensjahr.
Für folgende Medizinprodukte der Anlage V AM-RL wurde die Befristung der Verordnungsfähigkeit verlängert bzw. geändert:
- Isotonische Kochsalzlösung zur Inhalation (Eifelfango), neu befristet bis zum 31. Dezember 2028
- VISMED®, neu befristet bis zum 16. Januar 2029
- HydroTouch, neu befristet bis zum 31. Dezember 2028.
Das Weitern wurden folgende Medizinprodukte aus der Anlage V gestrichen und sind somit nicht mehr verordnungsfähig:
- EtoPril®
- Klistier Fresenius.
Impfstoffe
Neuer COVID-19-Impfstoff Comirnaty KP.2 – Bestellung und Abrechnung
Der neue, an die Omikron-Variante KP.2 angepasste Impfstoff von Biontech/Pfizer wird ab dem 11. November erstmals ausgeliefert. Die Bestellfrist dafür läuft bis zum 5. November.
Biontech/Pfizer stellt damit künftig einen weiteren an die Omikron-Variante KP.2 angepassten neuen COVID-19-Impfstoff bereit.
- Arztpraxen können Comirnaty KP.2 ab sofort bestellen
- die an JN.1 angepassten Comirnaty-Impfstoffprodukte sind weiterhin erhältlich
- Das Robert Koch-Institut (RKI) gibt an, dass sich die beiden Varianten JN.1 und KP.2 nur minimal durch drei Mutationen im Spike-Protein unterscheiden -> Es sei daher davon auszugehen, dass beide variantenangepassten Impfstoffe vergleichbar gut schützen.
Comirnaty KP.2 kann wie JN.1
- zur Grundimmunisierung
und - für Auffrischimpfungen
eingesetzt werden.
Nach Angaben des Zentrums für Pandemie-Impfstoffe und -Therapeutika (ZEPAI) steht das neue Vakzin wie bisher in drei Dosierungsstärken zur Verfügung
- für Personen ab zwölf Jahren,
- für 5- bis 11-Jährige
- sowie für Säuglinge und Kleinkinder ab sechs Monaten bis vier Jahre.
Hinweise zur Bestellung
- Bestellung bis Dienstag, 5. November, 12 Uhr, bei Ihrer Wahlapotheke
- Rezept mit Impfstoffnamen, zum Beispiel beim Vakzin für ab 12-Jährige „Comirnaty 30 Mikrogramm/Dosis KP.2“, sowie die benötigte Menge an.
- Kostenträger Bundesamt für Soziale Sicherung (BAS) mit IK 103609999
- Keine Unterscheidung bei der Bestellung zwischen gesetzlich oder privat versicherten Personen
Hinweise zum Impfstoff
- Impfstoff für ab 12-Jährige (graue Kappe) -> als Fertiglösung
- Impfstoff für 5- bis 11-Jährige (blaue Kappe) -> als Fertiglösung
- keine Verdünnung mit NaCI-Lösung erforderlich
- Ein Vial enthält jeweils sechs Dosen des Vakzins
- Vakzin für Mädchen und Jungen im Alter von sechs Monaten bis vier Jahren muss vor der Verabreichung mit NaCl-Lösung verdünnt werden. Aus einem Vial (gelbe Kappe) können dann drei Dosen entnommen werden.
Abrechnung und Dokumentation
Die Impfung mit dem neuen Impfstoff „Comirnaty KP.2“ kann mit Verfügbarkeit in den Praxen ab 11.11.2024 mittels der neuen Symbolnummern 88348A, 88348B, 88348R, 88348V, 88348W bzw. 88348X über die KV Berlin abgerechnet werden.
Eine Meldung der durchgeführten Impfungen ist seit 1. Juli nicht mehr erforderlich. Die Dokumentation erfolgt wie bei anderen Impfungen auch in der Patient:innenakte sowie im Impfausweis.
ZEPAI: Kein Regressrisiko für Ärzt:innen
- Es stehen wie bisher nur Mehrdosenbehältnissen und keine Einzeldosen zur Verfügung
- Der Bund wird daher weiterhin keine Regressansprüche erheben,
- sollten trotz bedarfsgerechter Bestellung oder sorgfältiger Terminplanung Impfstoffdosen verfallen oder
- weniger als beispielsweise sechs Impfstoffdosen aus einem Mehrdosisbehältnis entnommen werden.
- Regressansprüche der Krankenkassen können in diesem Zusammenhang nicht entstehen, da der zentral beschaffte Impfstoff durch den Bund weiterhin kostenlos zur Verfügung gestellt wird.
Ausführliche Informationen zum neuen Impfstoff – u. a. zu Angaben auf dem Rezept, Impfzubehör, Haltbarkeit und Lagerung – hat die KBV zusammengefasst.
Das Impfzubehör (Spritzen, Kanülen) bestellen Sie bitte wie bei anderen Impfstoffen auch über einen geeigneten Leistungserbringenden.
Influenza-Impfung-Wechsel quadrivalent zu trivalent
Mit dem Beschluss vom 3. September 2024 hat der Gemeinsame Bundesauschluss in den Hinweisen zur Umsetzung zur Influenza-Impfung in der Schutzimpfungs-Richtlinie (SI-RL) die Streichung des Wortes „quadrivalent“ und somit einer Nicht-Spezifizierung der Influenza-Impfung beschlossen.
Dieser Beschluss ist am 27. September 2024 nach Veröffentlichung im Bundesanzeiger in Kraft getreten.
Hintergrund der Änderung ist eine Empfehlung der Weltgesundheitsorganisation (WHO). Die WHO veröffentlicht jedes Jahr eine Empfehlung, welche Antigenkombination für Influenza-Impfstoffe für die kommende Impfsaison verwendet werden soll. Für die diesjährige Saison hat die WHO den Wechsel von quadrivalent zu trivalent empfohlen. Der quadrivalente Impfstoff wird allerdings noch nicht ausgeschlossen, da eine Zusatzempfehlung für den Stamm der zweiten B-Linie vorliegt.
Die Ständige Impfkommission (STIKO) übernimmt die Empfehlung der WHO, mit der Ausnahme der nicht konkreten Empfehlung des trivalenten Influenza-Impfstoffes, sondern je nach betroffener Personengruppe einen inaktivierten Hochdosis-Influenza-Impfstoff/Influenza-Impfstoff mit aktueller von der WHO empfohlener Antigenkombination.
Da in der SI-RL mit dem Beschluss vom 3. September 2024 keine Spezifizierung des Impfstoffes erfolgt, ist die Impfung mit dem quadrivalenten Impfstoff weiterhin zu Kassenlasten möglich.
Schutzimpfungs-Richtlinie ─ Impfungen aufgrund Reiseindikation (beruflich)
In der Anlage 1 der Schutzimpfungs-Richtlinie (SI-RL) des Gemeinsamen Bundesausschusses (G-BA) sind auch Impfungen mit Reiseindikation aufgeführt.
Bei einigen Impfungen wird in der Spalte „Hinweise zur Umsetzung“ darauf hingewiesen, dass ein Leistungsanspruch aufgrund von Auslandsaufenthalten nur im Rahmen des § 11 Absatz 3 der SI-RL besteht:
„Versicherte haben nur dann Anspruch auf Leistungen für Schutzimpfungen nach Absatz 1, die wegen eines erhöhten Gesundheitsrisikos durch einen Auslandsaufenthalt indiziert sind, wenn
- der Auslandsaufenthalt beruflich oder durch eine Ausbildung bedingt ist,
oder- entsprechend den Hinweisen in Anlage 1 zum Schutz der öffentlichen Gesundheit ein besonderes Interesse daran besteht, der Einschleppung einer übertragbaren Krankheit in die Bundesrepublik Deutschland vorzubeugen.“
Somit sind diese Impfungen nur dann eine Leistung der Gesetzlichen Krankenversicherung, wenn der Auslandsaufenthalt beruflich, ausbildungsbedingt ist oder die Einschleppung einer übertragbaren Krankheit nach Deutschland verhindert werden soll.
Impfungen für private Urlaubsreisen sind somit keine Kassenleistung. Satzungsleistungen einzelner Krankenkassen können Ergänzungen zur SI-RL enthalten.
Bitte beachten Sie bei jeder Impfung (zusätzlich zur Indikation) die Hinweise zur Umsetzung, ob für Ihre Patient:in die Voraussetzung für eine Impfung zu Kassenlasten besteht.
Bei bestehendem Anspruch, wird auch der Impfstoff für die Reiseindikation über den Sprechstundenbedarf (SSB) bezogen:
- auch im Einzelfall
- auch bei Bezug nur einer Impfdosis
- Kreuz bei 8+9 auf dem Muster 16
- Ohne Nennung von Versichertennamen
- analog aller anderen Impfungen der SI-RL
Zur Information: Der Bezug des Impfstoffes gegen Denguefieber über den SSB sowie die Abrechnung der ärztlichen Leistung per eGK ist derzeit nicht möglich → es fehlt weiterhin eine entsprechende Impfvereinbarung über das ärztliche Honorar → daher Privatverordnung und GOÄ → Erstattung durch die Krankenkasse.
RSV-Impfung für über 75jährige in Schutzimpfungs-Richtlinie aufgenommen
Der Gemeinsame Bundesausschuss (G-BA) hat per Beschluss am 3.9.2024 die Aufnahme der Impfung gegen das Respiratorische Synzytial Virus (RSV) in die Schutzimpfungs-Richtlinie (SI-RL) vorgenommen. Der Beschluss trat am 27.09.2024 in Kraft. Zuvor hatte die Ständige Impfkommission (STIKO) die Empfehlung zur RSV-Impfung für Personen über 75 und Personen zwischen 60 und 74 Jahren mit bestimmten Risikofaktoren ausgesprochen.
| Impfung gegen | Indikation | Hinweise zur Umsetzung |
| 1 | 2 | 3 |
| „Respiratorische Synzytial-Viren (RSV) | Standardimpfung: | Einmalige Impfung möglichst vor Beginn der RSV-Saison mit einem proteinbasierten RSV-Impfstoff. Auf Basis der aktuellen Datenlage kann noch keine Aussage zur Notwendigkeit von Wiederholungsimpfungen getroffen werden. |
Indikationsimpfung:
2. Bewohnende von Einrichtungen der Pflege ab dem Alter von 60 Jahren. | Einmalige Impfung möglichst vor Beginn der RSV-Saison mit einem proteinbasierten RSV-Impfstoff. Auf Basis der aktuellen Datenlage kann noch keine Aussage zur Notwendigkeit von Wiederholungsimpfungen getroffen werden. Leichte oder unkomplizierte bzw. medikamentös gut kontrollierte Formen der genannten chronischen Erkrankungen gehen nach jetzigem Wissensstand nicht mit einem deutlich erhöhten Risiko für einen schweren RSV-Krankheitsverlauf einher." |
Die Impfung gegen RSV wurde mit einer Vergütung von 83,6 Punkten (derzeit 9,98 Euro) aufgenommen und kann ab sofort unter Angabe der Symbolnummern 89137 (Standardimpfung) und 89138 (Indikationsimpfung) über die KV Berlin abgerechnet werden.
Bitte beachten Sie, dass die Abrechnungsziffern nach aktuellem Stand möglicherweise noch nicht in Ihr Praxisverwaltungssystem eingepflegt sind und ggf. durch Sie eingetragen werden müssen.
Die zugelassenen RSV-Impfstoffe (Abrysvo® oder Arexvy® beide preislich gleich und für den Personenkreis aus der SI-RL zugelassen) können seit Stichtag 1. Oktober 2024 zu Lasten des Sprechstundenbedarfs in der Apotheke bestellt werden.
Schwangere und Säuglinge sind von der SI-RL bezüglich der RSV-Impfung nicht umfasst.
Informationsquellen: Impfvereinbarung der KV Berlin
Wirtschaftlichkeitsprüfung
Durchschnittswerteprüfung – Update regionale Praxisbesonderheiten
Seit 2020 wird in Berlin die Durchschnittswerteprüfung als statistische Auffälligkeitsprüfung durchgeführt.
Im Zuge der Umstellung von der Richtgrößenprüfung auf die Durchschnittswerteprüfung wurden Arzneimittelziele als Teil der Arzneimittelvereinbarung eingeführt. Die aktuellen Informationen zu den Zielen und zur Quotenhöhe finden Sie in den Verordnungs-News Nr. 6 2024.
Die regionalen Praxisbesonderheiten wurden beim Wechsel der Prüfart ebenfalls angepasst. Die befristeten Praxisbesonderheiten im Bereich Arzneimittel und Heilmittel sind nach einmaliger Verlängerung ausgelaufen, sodass aktuell ausschließlich die nachfolgend aufgeführten Praxisbesonderheiten im Bereich Arzneimittel zur Anwendung kommen.
- Verordnungskosten der ab 2014 neu zugelassenen Arzneimittel zur Behandlung der chronischen Hepatitis C nur bei enger Indikationsstellung und nach abgeschlossenem Nutzenbewertungsverfahren.
- Enzymersatztherapie und Arzneimittel bei seltenen Krankheiten (Orphan drugs) mit folgenden Wirkstoffen: Agalsidase alfa, Agalsidase beta, Algucosidase alfa, Amifampridin, C1-Inhibitor, Elo-sulfase, Eltrombopag, Galsulfase, Icatibant, Imigluverase, Idursulfase, Laronidase, Carglumsäure, Mercatamin, Miglustat, Natrium-Phenylbutyrat, Nitisinon, Romiplostim, 4-HydroxybuttersäureNa-Salz, Sapropterin, Velaglucerase
- Substitution von Plasmafaktoren bei Faktormangelkrankheiten bei fachärztlichen Internisten mit SP Hämatologie und Onkologie (HUG 2000, 2002, 2010 und Ärzte mit Abrechnungsgenehmigung Onkologie der HUG 110, 112, 117, 130, 1700, 1702, 1707)
- Wachstumshormonbehandlung bei Kindern mit nachgewiesenem Minderwuchs
- Hormonelle Behandlung und In-vitro-Fertilisation zum Herbeiführen einer Schwangerschaft
- nach strenger Indikationsstellung gemäß den Richtlinien über künstliche Befruchtung bei Repro-duktionsmedizinern (HUG 1300, 1307).
- Arzneimitteltherapie der Mukoviszidose
- Palivizumab zur Prävention von RSV-Erkrankungen
- Immunsupressiva nur nach Organtransplantation, Eingrenzung auf Arzneimittel ausschließlich für diese Indikation
- Asthmatherapeutika für Kinderärzte
- Parenterale Ernährung nur mittels Fertigarzneimitteln
- Hyposensibilisierungen
Sofern Sie Verordnungskosten für Arzneimittel aus den oben aufgeführten Bereichen haben, werden die Mehrkosten (über dem Vergleichsgruppendurchschnitt) bei der Durchschnittswerteprüfung von Amts wegen abgezogen.
Darüber hinaus können individuelle Praxisbesonderheiten an die Prüfungsstelle gemeldet werden. Dies kann im Rahmen der Stellungnahme innerhalb eines eröffneten Prüfverfahrens erfolgen oder vorab als sogenannte „Vorabmeldung“. Informationen, die die Prüfungsstelle dafür benötigt, entnehmen Sie bitte dem Praxisleitfaden.
Wir empfehlen die Vorabmeldung frühestens nach Abschluss des Kalenderjahres vorzunehmen. Eine Berücksichtigung der Verordnungskosten im Prüfverfahren erfolgt ebenfalls über die Mehrkostenberechnung.
Der Vollständigkeit halber erwähnen wir hier auch die bundesweiten Praxisbesonderheiten, die im Rahmen der Durchschnittswerteprüfung berücksichtigt werden können. Dabei werden die Verordnungskosten für die entsprechenden Arzneimittel komplett herausgerechnet, wenn die zwischen GKV-Spitzenverband und dem jeweiligen pharmazeutischen Unternehmen vereinbarten Bedingungen für eine bundesweite Praxisbesonderheit eingehalten werden.
Bitte prüfen Sie die für Sie relevanten Arzneimittel hinsichtlich der Bedingungen wie notwendige Vortherapie, Schwere der Erkrankung, Patient:innenklientel, usw. Zur Unterstützung sind auf der Website der KV Berlin die bestehenden bundesweiten Praxisbesonderheiten aufgeführt.
Allgemeine Informationen zur Wirtschaftlichkeitsprüfung, zu den Arzneimittelzielen und den Praxisbesonderheiten (bundesweit, regional vereinbart und individuell) finden Sie hier.
Heilmittel
Flexiblere Zeitbezüge bei manueller Lymphdrainage seit 1. Oktober 2024
Die Heilmittel-Richtlinie definiert für die Verordnung von manueller Lymphdrainage grundsätzlich konkrete zeitliche Vorgaben.
Die Auswahl der Therapiezeit von 30, 45 oder 60 Minuten bemisst sich nach der Anzahl der zu behandelnden Körperteile und galt bislang als bedarfsgerecht. Dies entspricht jedoch nicht mehr dem heutigen medizinisch-therapeutischen Stand. Zudem kann der Bedarf an Therapiezeit bei der Verordnung nicht immer sicher abgeschätzt werden, da diese von vielen Faktoren wie von witterungsbedingten Einflüssen oder individuellen Belastungen abhängt.
In der Folge forderten Therapeut:innen in den Arztpraxen häufig Änderungen an Verordnungen ein, was erhebliche bürokratische Aufwände verursachte. Aufgrund dessen hat der Gemeinsame Bundesausschuss (G-BA) nun mit einer Änderung der Heilmittel-Richtlinie reagiert.
Der G-BA hat die Vorgaben der Heilmittel-Richtlinie geändert, die bislang für die Auswahl der Therapiezeit (Dauer einer Behandlung) zugrunde gelegt wurden.
Die neue Systematik richtet sich künftig vor allem nach dem Stadium des Lymphödems, weniger nach der Zahl der zu behandelnden Körperteile. Die Vertragsärzt:innen können manuelle Lymphdrainage dann aber auch ohne die Angabe der Therapiezeit verordnen. In diesem Fall entscheiden die Therapeut:innen, ob angesichts des jeweiligen Stadiums des Lymph- oder Lipödems und der Anzahl der betroffenen Körperteile 30, 45 oder 60 Minuten Therapiezeit erforderlich sind.
Überblick über die neuen stadienabhängigen Zeitvorgaben
MLD 30 min
bei Stadium I zur Behandlung von
- einem Körperteil (Kopf/Hals oder ein Arm oder ein Bein oder Rumpf) oder
- zwei Körperteilen (beide Arme oder beide Beine oder ein Arm und ein Bein oder eine Extremität und Kopf/Hals oder Rumpf)
bei Stadium II zur Behandlung von
- einem Körperteil (Kopf/Hals oder ein Arm oder ein Bein oder Rumpf)
MLD 45 min
bei Stadium I (in Ausnahmefällen bei kurzfristigem/vorübergehendem Behandlungsbedarf) zur Behandlung von
- zwei Körperteilen (beide Arme bzw. beide Beine oder ein Arm und ein Bein oder eine Extremität und Kopf/Hals oder Rumpf)
bei Stadium II zur Behandlung von
- einem Körperteil (Kopf/Hals oder ein Arm oder ein Bein oder Rumpf) oder
- zwei Körperteilen (beide Arme oder beide Beine, ein Arm und ein Bein oder eine Extremität und Kopf/Hals oder Rumpf)
bei Stadium III zur Behandlung von
- einem Körperteil (Kopf/Hals oder ein Arm oder ein Bein oder Rumpf)
MLD 60 min
bei Stadium II zur Behandlung von
- zwei Körperteilen (beide Arme oder beide Beine oder ein Arm und ein Bein oder eine Extremität und Kopf/Hals oder Rumpf)
bei Stadium III zur Behandlung von
- einem Körperteil (Kopf/Hals oder ein Arm oder ein Bein oder Rumpf) oder
- zwei Körperteilen (beide Arme oder beide Beine oder ein Arm und ein Bein oder eine Extremität und Kopf/Hals oder Rumpf)
MLD ohne Therapiezeit als erweiterte Verordnungsmöglichkeit
Ebenso können Praxen seit dem 1. Oktober MLD ohne Therapiezeitangaben verordnen – mit oder ohne Kompressionsbandagierung. Über die Therapiezeit entscheiden dann befundabhängig die Therapeut:innen.
Im Heilmittelkatalog wurden daher in der Diagnosegruppe „LY – Lymphabflussstörungen“ die beiden vorrangigen Heilmittel „MLD“ und „MLD + Kompressionsbandagierung“ aufgenommen.
Für die Verordnung von MLD ohne Therapiezeit ist die Angabe des Stadiums des Lymph- oder Lipödems in Form des ICD-10-Codes erforderlich. Das Praxisverwaltungssystem lässt eine Verordnung ohne Zeitvorgabe nur dann zu, wenn der ICD-10-Code endständig ist und somit die Angabe zum Stadium des Ödems enthält. Die Angabe der zu behandelnden Körperteile auf der Verordnung ist nicht mehr erforderlich. Wie bei allen physiotherapeutischen Maßnahmen können bis zu drei vorrangige (MLD-)Heilmittel auf einer Verordnung kombiniert werden.
Wirtschaftlichkeitsprüfungsrelevanz
MLD wird in den meisten Behandlungsfällen von Lymph- und Lipödemen erst ab Stadium II verordnet. Verordnungen für diese Indikationen gelten als langfristiger Heilmittelbedarf (LF) bzw. besonderer Verordnungsbedarf (BVB) und unterliegen nicht der statistischen Wirtschaftlichkeitsprüfung (Diagnoseliste der Kassenärztlichen Bundesvereinigung).
Ödeme im Rahmen von bösartigen Neubildungen (ICD-10-Bereich C00–C97) gelten stadienunabhängig als LF. Diese Kosten fließen ebenfalls nicht in das Verordnungsvolumen Ihrer Praxis ein und unterliegen somit nicht der Durchschnittswerteprüfung. Hinweis: Um auch hier eine Verordnung von MLD ohne Zeitvorgabe auszustellen, muss zusätzlich ein ICD-10-Code angegeben werden, aus dem das Stadium des Lymphödems hervorgeht.
Hingegen unterliegen Verordnungen auf Grundlage von ICD-10-Codes mit Lymphödem im Stadium I oder ohne Angabe des Stadiums der statistischen Wirtschaftlichkeitsprüfung.
Bei der Verordnung von MLD ohne Zeitangabe handelt es sich definitionsgemäß nicht um eine Blankoverordnung gemäß §125a SGB V. Die Verantwortung für die Wirtschaftlichkeit bleibt bei den verordnenden Ärzt:innen.
Den Beschluss des G-BA finden Sie hier.
Erweiterung der Heilmittel-Diagnoseliste ab 1. Oktober 2024
Zum 1. Oktober 2024 wurde die Diagnoseliste zum langfristigen Heilmittelbedarf (Anlage 2 der Heilmittel-Richtlinie) sowie zu den bundesweit geltenden besonderen Verordnungsbedarfen für Heilmittel erweitert.
Änderungen beim langfristigen Heilmittelbedarf
Aus dem Bereich Lungenkrankheiten kommen
- J84.10 „Sonstige interstitielle Lungenkrankheiten mit Fibrose, ohne Angabe einer akuten Exazer-bation“
und - J84.80 „Sonstige nähere bezeichnete interstitielle Lungenkrankheiten, ohne Angabe einer akuten Exazerbation“ – im Bereich der Diagnosegruppe „AT“ Atemtherapie (Physiotherapie)
hinzu.
Langfristiger Heilmittelbedarf ist für schwerkranke Patient:innen vorgesehen, die voraussichtlich einen Behandlungsbedarf mit Heilmitteln von mindestens einem Jahr benötigen. Verordnungen im Rahmen des langfristigen Heilmittelbedarfs unterliegen nicht der statistischen Wirtschaftlichkeitsprüfung (Heilmitteldurchschnittswerteprüfung). Demnach fließen die Kosten dieser Verordnungen nicht in das Verordnungsvolumen der Praxis ein.
Änderungen bei den besonderen Verordnungsbedarfen
Aus dem Bereich der entzündliche Myopathien kommt
- G72.4 „Entzündliche Myopathie, andernorts nicht klassifiziert“
hinzu.
Die Verordnung ist in den Diagnosegruppen
„PN“/“AT“ (Physiotherapie),
„EN3“ (Ergotherapie) sowie
„SC“/“SP6“ (Stimm-, Sprech-, Sprach- und Schlucktherapie) möglich.
Besondere Verordnungsbedarfe sind für schwerkranke Patient:innen gedacht, die in der Regel für einen bestimmten Zeitraum eine intensive Behandlung mit Heilmitteln benötigen. Die Verordnungskosten fließen zunächst in das Verordnungsvolumen der Praxis ein und werden im Falle eines Prüfverfahrens berücksichtigt und abgezogen.
Bei den neu hinzugekommenen Indikationen können Sie von der geltenden Höchstmenge je Verordnung gemäß Heilmittelkatalog abweichen und die notwendigen Heilmittel ab der ersten Verordnung für einen Zeitraum von zwölf Wochen verordnen. Dies gilt analog für die Weiterverordnungen.
Die KBV hat die Stammdaten für die Verordnungssoftware zum 1. Oktober angepasst. Der Beschluss des G-BA trat zum 1.Oktober in Kraft.
Blankoverordnung für Physiotherapie im Schulterbereich ab 1. November
Seit April 2024 ist es möglich, für Ergotherapie eine Blankoverordnung auszustellen, siehe Verordnungs-News 03/2024.
Ab November 2024 sind Blankoverordnungen nun auch für den Bereich der Physiotherapie bei Diagnosen im Schulterbereich ausstellbar.
Die Praxissoftware prüft ab 1. November 2024, ob die eingegebene Diagnose zu einer Blankoverordnung berechtigt.
Spricht aus medizinischer Sicht nichts dagegen, klicken Ärztinnen und Ärzte dies entsprechend an. Die Software kennzeichnet die Heilmittel-Verordnung dann als Blankoverordnung und lässt die Felder für Heilmittel, Frequenz und Menge offen.
Grundsätzliche zur Blankoverordnung
Die Verträge zu Blankoverordnungen werden zwischen GKV-Spitzenverband und der Kassenärztlichen Bundesvereinigung getroffen.
Im Rahmen einer Blankoverordnung erfolgt die Diagnose durch Ärzt:innen oder Psychotherapeut:innen. Die Entscheidung über die Auswahl des Heilmittels sowie die Festlegung der Anzahl und Frequenz obliegt dann den Physio- und Ergotherapeut:innen. Diese Regelung soll zu einer gesteigerten Flexibilität und Verantwortung der Heilmittelerbringenden führen, da sie individueller auf den Behandlungsverlauf eingehen können.
Die Verantwortung für diese Entscheidungen liegt bei den Therapeut:innen, die die Therapie flexibel anpassen können. Die Verordnung bleibt maximal 16 Wochen gültig. Nach Ablauf dieser Frist entscheiden die behandelnden Ärzt:nnen den weiteren Therapieverlauf.
Wirtschaftliche Verantwortung
Ein wesentlicher Unterschied zur herkömmlichen Verordnung ist, dass Blankoverordnungen nicht der vertragsärztlichen Wirtschaftlichkeitsprüfung unterliegen. Das bedeutet, dass die finanzielle Verantwortung für die Menge, Art und Frequenz der Behandlung auf die behandelnden Therapeut:innen übergeht. Ärzt:innen und Psychologische Psychotherapeut:innen haben jedoch weiterhin die Möglichkeit, sich gegen eine Blankoverordnung zu entscheiden und bestimmen damit weiter selbst über die Therapiedetails.
Weitere Informationen finden Sie bei der KBV.
Sprechstundenbedarf
Glucose-Toleranztest
In den Verordnungs-News November 2022 und Februar 2023 informierten wir bereits über die auf dem Markt befindlichen Glucose- Fertiglösungen zur Glucosetoleranztestung.
Bitte beachten Sie bei der Auswahl eines Präparates auf das Wirtschaftlichkeitsgebot. Die Herstellung einer trinkfertigen Glucose-Lösung als Rezeptur in der Apotheke wird als unwirtschaftlich gesehen.
Nähere Informationen zur Verordnung von Rezepturen finden Sie in den Verordnungs-News März 2024.
Außerdem sind Glucosepräparate mit der Klassifizierung Lebensmittel keine Kassenleistung.
Übersicht Glucose-Lösungen
| Artikelname | Packungsgröße | PZN | Bruttopreis |
| GLUCOSETEST oGTT InfectoPharm 27,5 g/100 ml Lösung | 2 x 100 mL | 18319713 | 10,97 € |
| GLUCOSETEST oGTT InfectoPharm 27,5 g/100 ml Lösung | 300 mL | 18319742 | 8,98 € |
| GLUCOSETEST oGTT InfectoPharm 27,5 g/100 ml Lösung | 15 x 300 mL | 18747142 | 105,52 € |
| GLUCOSE-Toleranztest 25 g/100 ml Lösung | 200 mL | 18447121 | 8,58 € |
| GLUCOSE-TOLERANZTEST 25 g/100 ml Lösung | 300 mL | 17874542 | 9,38 € |
| GLUCOSE-TOLERANZTEST Glucex 27,5 g/100 ml Lösung | 300 mL | 18827533 | 9,34 € |
Stand 15. Oktober 2024
Sonstiges
Krankenbeförderung per Videosprechstunde: Neue Regelungen seit September 2024
Am 19. September 2024 hat der Gemeinsame Bundesausschuss (G-BA) festgelegt, unter welchen Voraussetzungen Krankenbeförderung per Videosprechstunde möglich ist. Die Verordnung per Videosprechstunde ist bereits für Heilmittel, häusliche Krankenpflege und medizinische Rehabilitation möglich.
Voraussetzungen für die Verordnung per Videosprechstunde
Für die Verordnung von Krankenbeförderung per Videosprechstunde gelten folgende Bedingungen:
- die Patientin oder der Patient muss in der Praxis bereits persönlich bekannt sein
- medizinische Voraussetzungen für die Krankenbeförderung müssen per Videosprechstunde sicher beurteilbar sein
Telefonische Verordnung
Sind alle relevanten Informationen durch eine unmittelbare Behandlung oder eine Videosprechstunde bekannt, kann in Ausnahmefällen auch eine Krankenbeförderung nach telefonischem Kontakt verordnet werden.
Wichtig zu beachten ist, dass patient:innenseitig kein Anspruch auf eine Verordnung per Videosprechstunde oder telefonisch besteht.
Die Kosten für Fahrten zu ambulanten oder stationären Behandlungen werden bei medizinischer Not-wendigkeit von den gesetzlichen Krankenkassen übernommen. Der G-BA regelt in der Krankentransport-Richtlinie die genauen Voraussetzungen und die Angaben zur Verordnung von Krankenfahrten und Krankentransporten.


